추상적인
AuNR과 PPTT의 도입은 세포골격과 세포 사이의 연결에 영향을 미쳐 암세포의 집단 이동을 억제할 수 있습니다. 초고해상도 현미경을 사용한 STORM 분석을 통해 액틴 세포골격의 파괴를 관찰했으며, 다른 현미경을 사용하여 최대 200배 확대 실험에서 DIC 이미지를 기록했습니다. 연구 결과, 인테그린 표적 AuNR과 세포 간 상호작용이 인산화 변화를 유발할 수 있음을 보여주었습니다. 세포골격 필라멘트와 세포 연결의 핵심 구성 요소인 인테그린의 형태 또는 발현 수준의 변화는 종양 이동을 억제하는 것으로 나타났습니다.
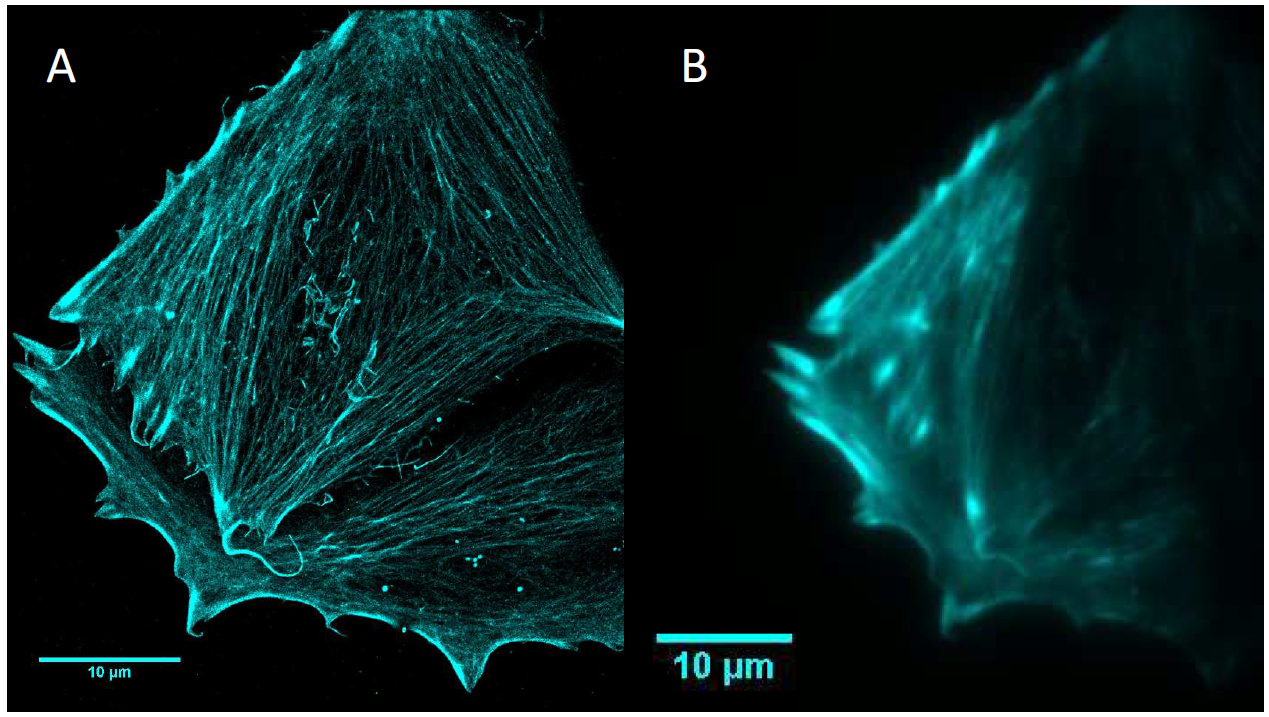
그림 1. 액틴 필라멘트에 대한 STORM(A)과 기존 형광 현미경 이미징(B)의 해상도 비교.
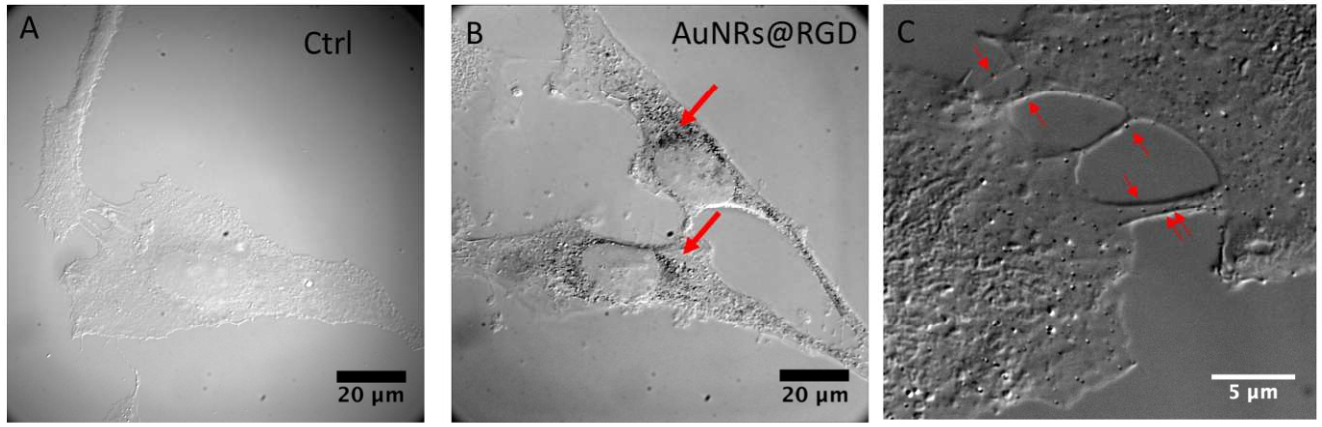
그림 2. AuNRs 처리에 따른 세포 흡수, 세포독성 및 운동성. (AB) 차등
간섭 대비(DIC) 현미경으로 관찰한 HeLa 세포의 이미지 (A)는 (없음)에서, (있음)에서
(B) 24시간 배양 후 AuNRs@RGD의 분포. (C) 24시간 배양 후 세포 접합 부위에 분포된 AuNRs@RGD의 DIC 이미지.
영상 기술 분석
기존의 형광 현미경은 광학 회절의 한계를 극복하기 어려워 금 나노로드와 PPTT가 세포에 미치는 영향을 관찰할 수 없으며, 초고해상도 장비 없이는 이미지를 얻는 것이 불가능합니다.디야나 95그리고400BSI본 애플리케이션에 이상적인 두 가지 소형, 고성능, 유연성을 갖춘 sCMOS 카메라가 사용되었습니다. 이 카메라는 CMS 저잡음 판독 모드와 고동적 모드를 포함한 다양한 모드를 제공합니다. 백샷 sCMOS는 거의 완벽한 95%의 양자 효율을 달성할 뿐만 아니라 2인치와 같은 넓은 시야각을 제공합니다. 200~1100nm의 넓은 스펙트럼 응답은 11μm 대형 화소의 감도와 동적 범위를 향상시키는 데 도움이 되며, 이는 다른 sCMOS 카메라에서는 찾아보기 힘든 장점입니다. 따라서 시료의 광손상 및 광표백 없이 낮은 조도와 짧은 노출 시간으로 장시간 이미징을 수행할 수 있습니다.
참고 자료
Wu Y, Ali MRK, Dong B, Han T, Chen K, Chen J, Tang Y, Fang N, Wang F, El-Sayed MA. 금 나노로드 광열 치료는 암세포 집단 이동을 억제하기 위해 세포 접합부 및 액틴 네트워크를 변화시킨다. ACS Nano. 2018년 9월 25일;12(9):9279-9290. doi: 10.1021/acsnano.8b04128. Epub 2018년 8월 27일. PMID: 30118603; PMCID: PMC6156989


 2022년 3월 3일
2022년 3월 3일